日本科学家Lijima于1991年发现碳纳米管(CNTs),现在碳纳米管被认为是学术领域和各工业领域的顶级研究课题。
这些纳米材料由石墨制成,是碳的同素异形体,结构通常为圆柱形,直径为纳米级,长度在数毫米范围内。它们的结构、机械和电子等性能非常优秀,这主要是由于它们的小尺寸、低质量、令人难以置信的机械强度以及高导电性和导热性。
碳纳米管最初被用作电子、光学、塑料和纳米技术领域内各种结构材料的添加剂。自21世纪初以来,碳纳米管已被引入药学和药物治疗学中的药物输送系统。
由于碳纳米管具有高比表面积、优异的化学稳定性和丰富的电子多环芳烃结构,使得材料能够吸附或偶联多种治疗分子(药物、蛋白质、抗体、DNA、酶等)。
现如今CNTs已被证明是一种极好的药物递送载体,它们可以通过直接渗透到细胞,然后在体内运输过程中保持药物完整而不进行新陈代谢。
许多同行研究已经表明,药物分子与CNT键合时,比传统运输⽅法能更有效、安全地输送到细胞中。这一奇妙的发现为药物制剂开辟了一条全新的途径,而且完全不同于以往制药工业中使用的传统技术。因此,碳纳米管某种程度彻底改变了以往的药理学理念。
CNTs首先被应用于抗肿瘤药物和抗生素药物开发,辅助癌症和感染治疗,后来CNT又被用于运输各种生物分子(基因、蛋白质、DNA、抗体、疫苗、生物传感器、细胞等),辅助基因治疗、免疫治疗、组织再生和不同疾病的诊断。
因此,在很短的时间内,碳纳米管就成为各学科研究人员关注的焦点,CNT可能成为未来具有预防疾病和保护健康的抗氧化剂,应用前景非常广泛。据悉,所有这些医学发现都处于实验阶段,仍未应用于临床实践。
碳纳米管:结构、类型和制备
碳纳米管(CNT)仅由碳原子组成,这些碳原子排列成一系列缩合的苯环,并卷成管状结构。这种新型人造纳米材料属于富勒烯家族,是碳的第三种同素异形体。其他两种同素异形体是石墨和金刚石,结构分别为天然sp2(平面)和sp3(立方)形式。
碳纳米管的结构根据层数分为两类:单壁碳纳米管(SWCNT)和多壁碳纳米管(MWCNT),如图1所示。
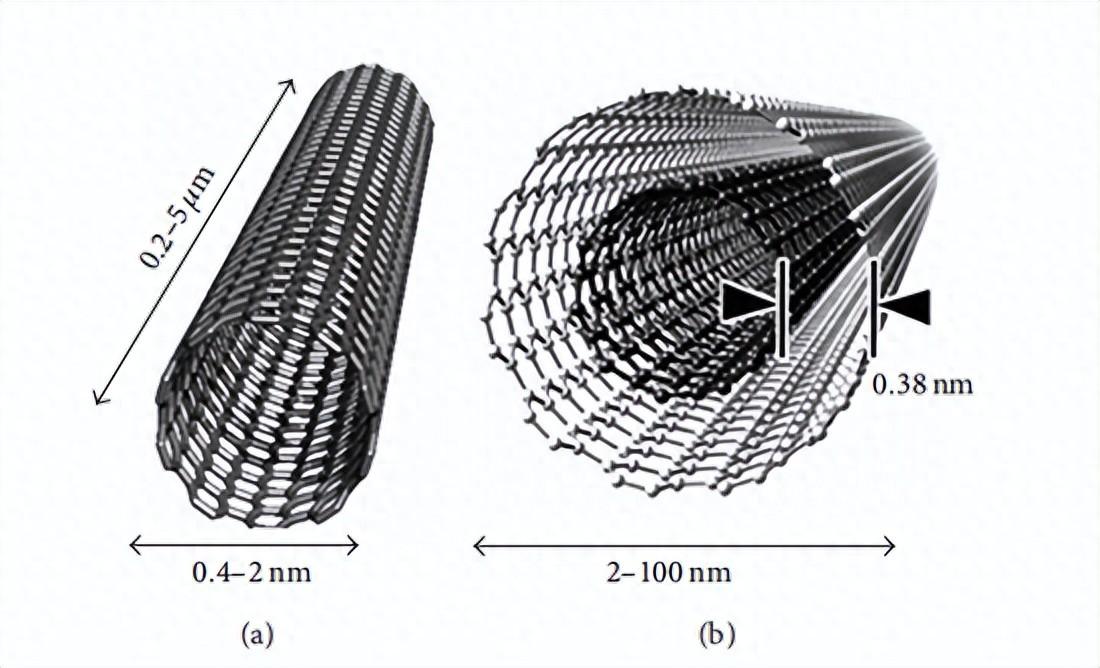
图1
SWCNT由直径在0.4和2nm之间的单个石墨烯圆柱体组成,通常以六角密排束形式出现(如图2)。 MWCNT由两个到数个同轴圆柱体组成,每个圆柱体由空心状的单个石墨烯制成。MWCNTs的外径范围为2—100nm,内径范围为1-3nm,长度为0.2至数米。
从化学反应的角度来看,CNT结构可分为两个区域:顶端和侧壁。控制这些独特性质的一个重要因素是石墨烯卷曲成管状所引起的结构变化。
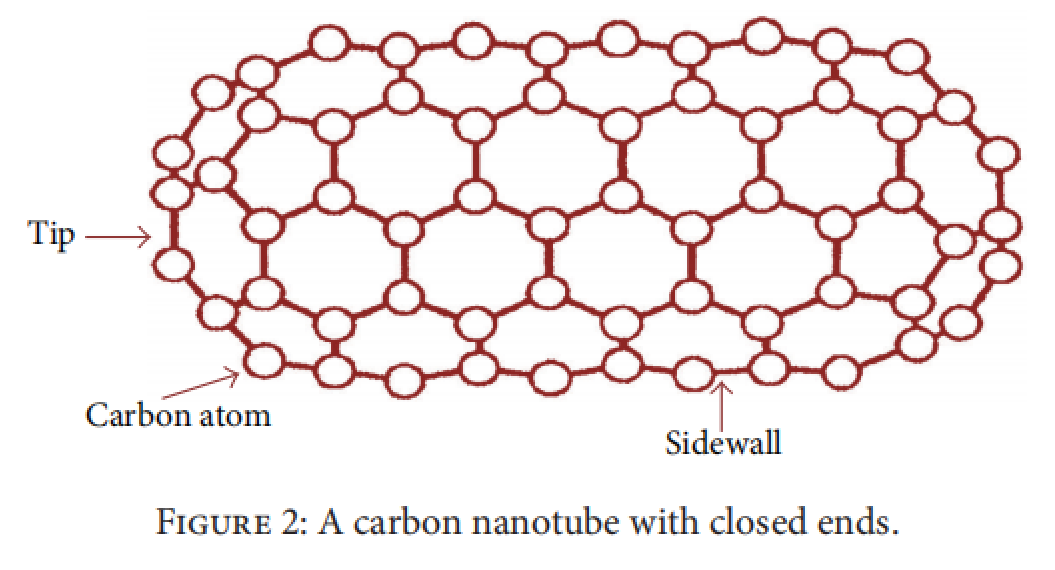
图2
另外,单壁碳纳米管和多壁碳纳米管的生产技术通常有三种:电弧放电法(使用两根碳棒的电弧气化)、激光烧蚀法(使用石墨)和化学气相沉积(使用碳氢化合物:CO、甲烷、乙烯、乙炔)。
碳纳米管的医学应用
1.生物医学应用
原始状态的碳纳米管并不能溶于水溶液,因为它们具有高度疏水的表面。为了增加CNT的水溶解性,我们需要对其表面进行功能化修饰,从而为其医学应用提供生物相容性和低毒性。
CNT的表面功能化通常有两种主要⽅法,即共价连接(化学键形成)和非共价连接(物理吸附)。至于实际应用中采用哪种方式,主要取决于和碳纳米管相连的生物分子性质。
CNT的共价连接功能化通常用强酸氧化来获得。在此过程中,羧基(‑COOH)基团在单壁碳纳米管或多壁碳纳米管的开口侧(尖端)和侧壁缺陷处形成,然后与氨基酸进一步共价结合。
为了在CNT的侧壁上生成–COOH,通常采用氮烯环加成,或使用重氮盐的芳基化/1,3‑偶极环加成。
图3是碳纳米管共价连接功能化的示意图。CNT的非共价功能化可以通过用两亲性表面活性剂分子或聚合物(聚乙二醇)涂覆CNT来实现。碳纳米管由于具有大型芳香族(‑电子)疏水表面,使其成为与互补分子和大生物分子(DNA)进行非共价相互作用的理想伙伴。
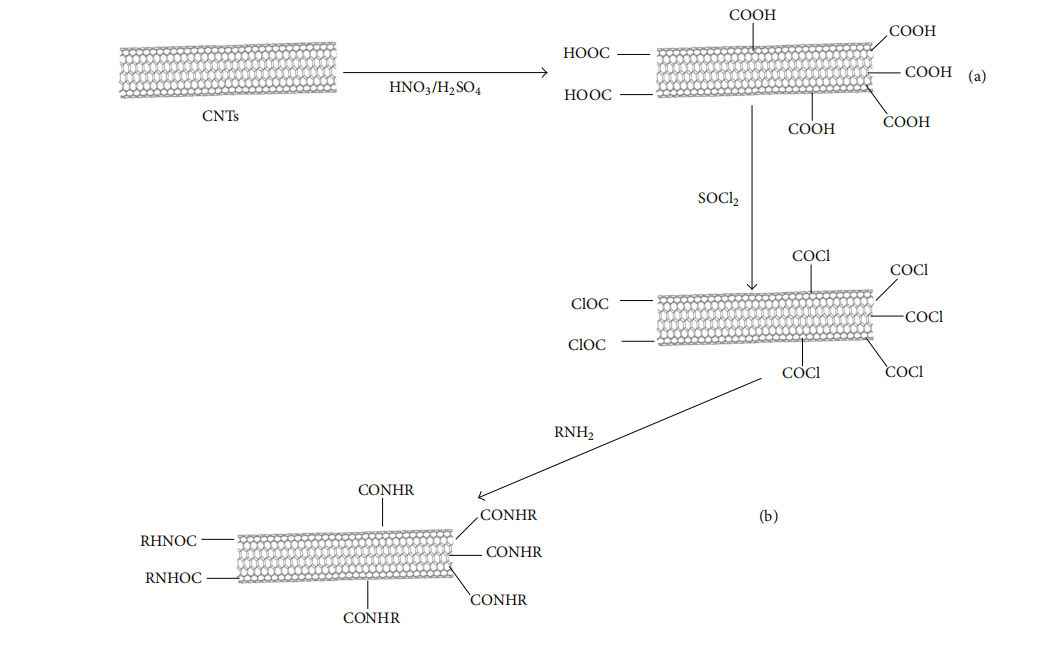
图3
图4是CNT的非共价功能化示意图。在功能化后,碳纳米管变成亲水性质,并能与药物或生物分子(基因、DNA、蛋白质、酶、生物传感器等)连接,以便将它们输送到靶细胞或器官中。
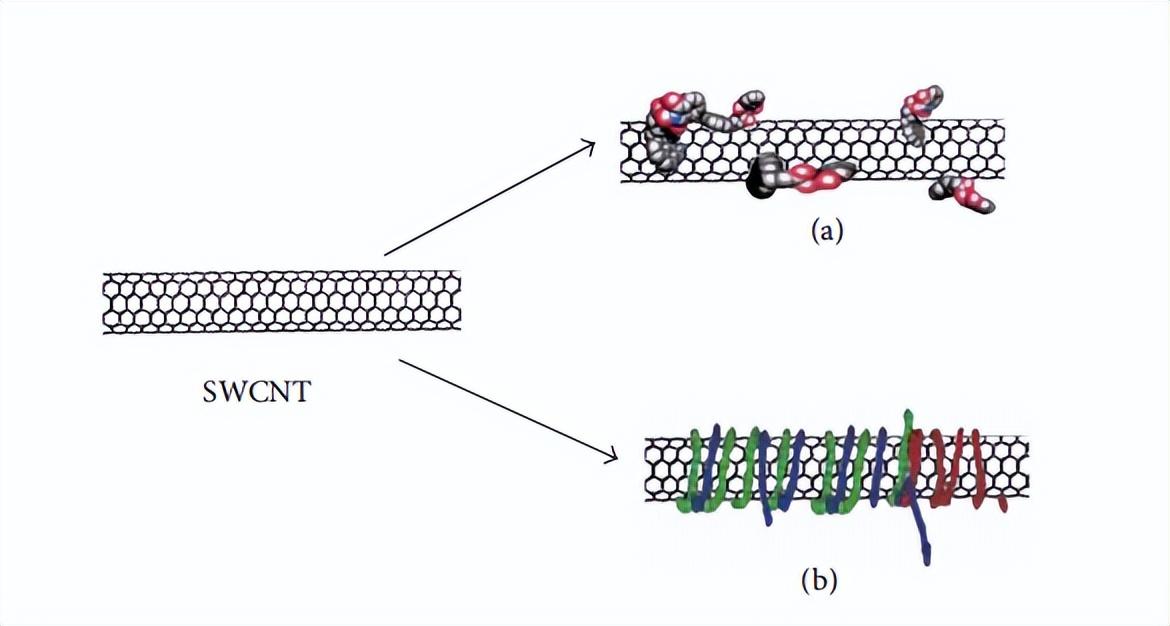
图4
2、碳纳米管在制药和医药⽅面的应用
碳纳米管在药学和医学中的主要应用包括药物合成、生物分子合成、细胞或器官的基因传递、组织再生以及生物传感器的诊断和分析。图5对CNT的医药应用进行了大致总结。
CNT输送药物的一般过程可以简要概括如下:科学家将药物固定在功能化碳纳米管的表面或内部,然后将获得的结合物通过经典的注射⽅式(口服、注射)引入动物体内,当然也可以通过使用磁性结合物直接引入目标部位。
例如,可以通过外部磁铁将药物引导到目标器官,如淋巴结。然后细胞会自动摄取药物CNT胶囊,最后纳米管将其包裹的药物成分分解到细胞中,从而完成药物传递。
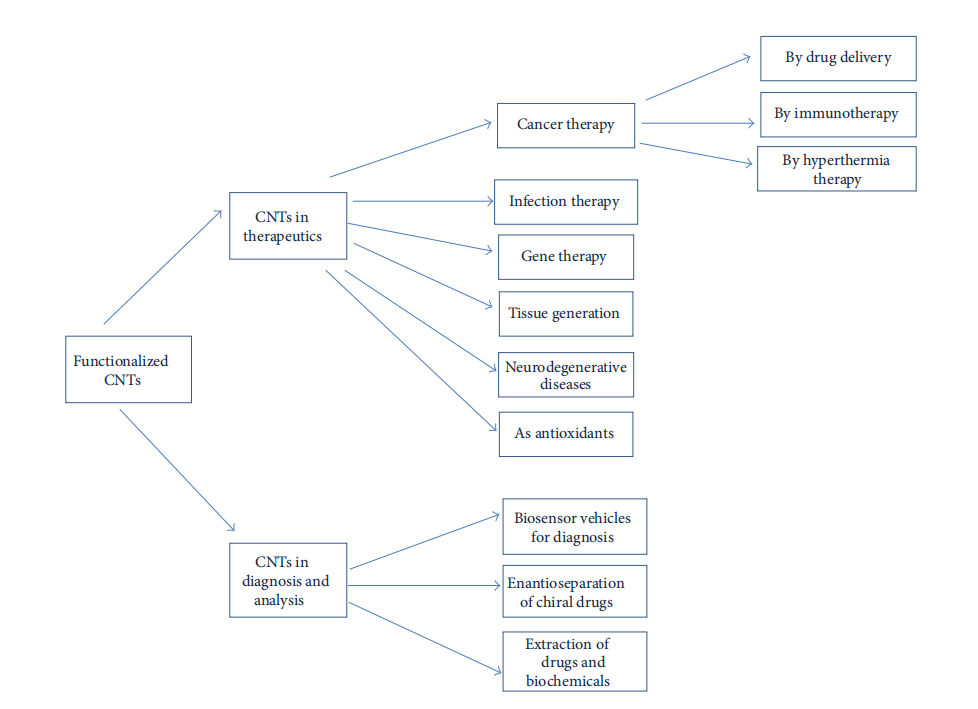
图5
图6示意图描述了药物的输送过程。通常,功能化的碳纳米管具有携带目标分子穿过细胞质膜和核膜的能力,并且不会对人体产生毒性副作用。因此,与单独使用传统药物制剂相比,将药物和CNT结合被证明是要更安全、更有效的输送方法。
药物到达靶细胞后,有两种可选释放溶解的方式:
第一种,药物进入细胞后,CNT载体留在细胞外面;第二种是药物和CNT载体都进入细胞内。
后一种内化吸收⽅法比第一种方法更为有效,这是因为载体进入细胞后,细胞内的生物环境可以降解药物和载体的结合物,以此实现原位释放药物分子。也就是说,药物是在细胞内部得到释放,而非细胞外面。
而在非内化方法中,药物输送方式不同。细胞外环境虽然有助于药物载体偶联物的降解,但药物需要穿过细胞的脂质膜才能进入细胞内部。因此,这种药物在穿透过程存在降解的可能性,从而降低药物治疗效果。
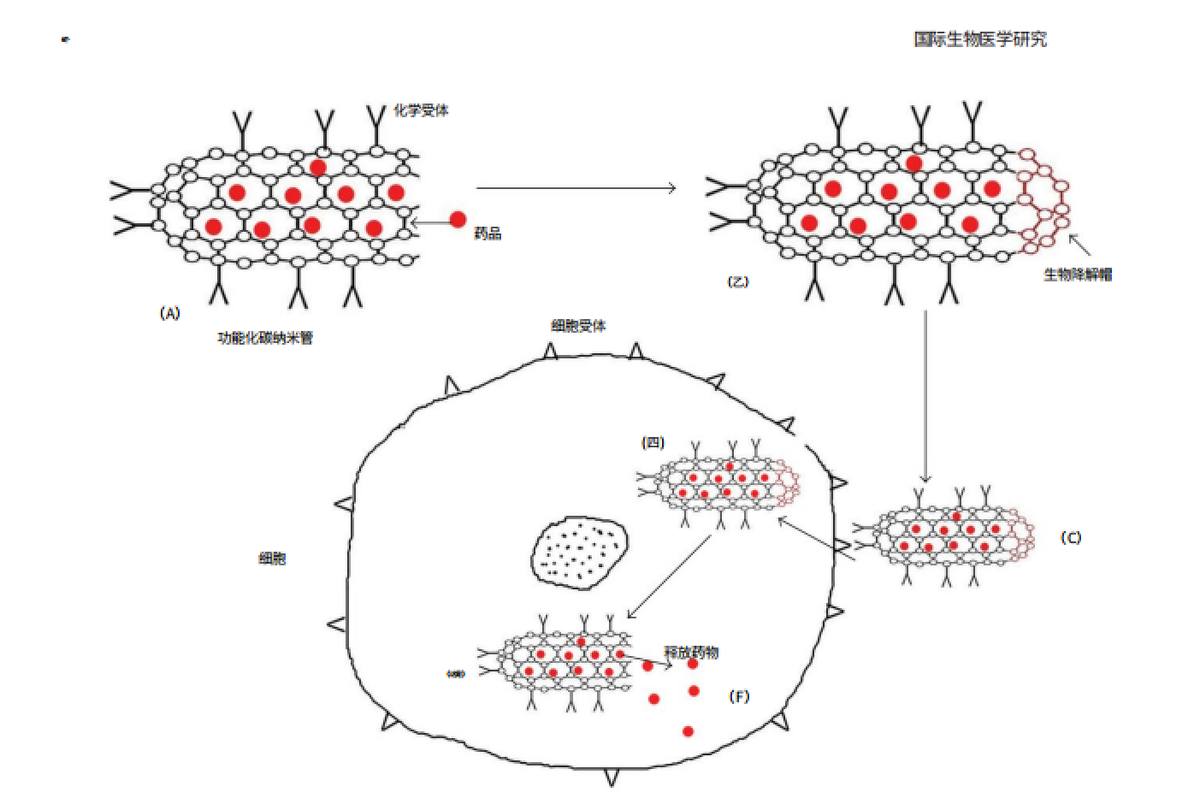
图6
碳纳米管的内化有两种机制:通过内吞途径或通过插入和扩散途径。
简而言之,碳纳米管具备跨细胞膜传递药物的能力,这些能力与其结构中的疏水相互作用、堆积相互作用、静电吸附和共价键有关,而且CNT还通过将药物吸附到空心圆柱体中,增加了药物吸附能力。
此外,碳纳米管不仅能够渗透到细胞中以促进治疗分子的细胞摄取,而且能够在运输和细胞渗透过程中保持它们的完整性。这一特性允许人体降低所用药物的剂量,从而减少毒性,特别是对于副作用较大的抗癌药物输送,效果更为显著。
碳纳米管的毒性分析
科学家对碳纳米管的体外毒理学进行了医学研究,通过分析水分散性单壁碳纳米管(SWCNT)在人肺细胞系A549内产生的体外细胞毒性影响,证实了SWCNT在A549细胞中没有进行细胞内定位,从而证明了SWCNT可以间接诱导出细胞毒性。
但是,人们也观察到用荧光素标记的水溶性单壁碳纳米管对小鼠B淋巴细胞和T淋巴细胞以及巨噬细胞并没有产生队形,而且保留了这些免疫细胞的免疫功能。
还有一些研究评估了两种直径的水溶性多壁碳纳米管(MWCNT)在C6大鼠神经胶质瘤细胞系中的潜在毒性和一般机制。
结果表明,较小尺寸的MWCNT似乎更比尺寸更大的CNT有毒。氧化应的增加可能导致了MWCNT在C6大鼠神经胶质瘤细胞中诱发出细胞毒性。
最近关于CNT毒性的研究也取得一些进展,通过IV或SC注射将SWCNT或MWCN注入到不同动物的胃肠道(大鼠、小鼠),从得到的毒性数据发现,在各种给药途径的评估中,CNT的生物医学应用具有低毒性。
只有当以聚乙二醇多壁碳纳米管(PEG‑MWCNT)形式在小鼠中注入非常高剂量药物(60mg/kg)时,CNT才会诱导出有意义的毒性。
尽管给药途径不同,单壁碳纳米管的毒性也与氧化应激密切相关。当CNT被用作皮下植入细胞生长的组织工程材料时,CNT仅仅诱发出一些非常有限的炎症,却表现出非常好的生物相容性并且没有产生任何严重的毒性。
当然科学家还没有对与治疗分子相关的功能化CNT进行临床实验研究,但是许多动物实验研究表明,CNT可能是许多CNT制备行业内工人职业性肺病的来源。
比如之前在人体中观察到的石棉病,科学家在几项锯齿动物上进行了相关研究,他们在动物气管内或咽内注入测试粉尘以评估CNT的肺毒性。这些研究人员得出结论,CNT能够在肺部产生炎症、上皮样肉芽肿、纤维化和生化变化。
在2013年,研究人员也发现,如果通过化学处理对其表面进行改性并减少碳纳米管有效长度,则可以完全缓解长期以来报道的石棉样反应性和致病性。
关于原始碳纳米管及其残留金属杂质的潜在毒性,目前科学界仍在研究中,并没有给出相关结论。
多壁碳纳米管(MWCNT)和石棉纤维之间明显的关联性也引发了人们的健康安全担忧。因此,尽管碳纳米管表现出在医疗治疗学⽅面巨大的潜在益处,CNT的毒性仍然是一个主要的应用难题,这仍然需要科学家更清楚地对其毒理进行探索和研究。
结论与展望
最近这些年碳纳米管在药学和医学不同领域中的应用取得了诸多进展,也具备许多独特的优势。
与传统药物输送方式相比,将这种纳米技术应用于生物领域,是更有效的替代方案,因为碳纳米管可以穿过细胞膜,并将药物、基因、生物分子、疫苗等深入到以前无法到达的靶细胞或器官中。另一种有前景的应用方式,也值得推广。
由于碳纳米管可以抵抗生物降解,人们可通过使用胶原蛋白碳纳米管材料作为组织生成和人工植入物的支架,用于修复缺陷器官,这比其他现有的材料都更有商业潜力。
将碳纳米管与生物传感器或其他材料的结合目前是治疗监测和疾病诊断以及不同领域药物分析的绝佳工具。产业应该重视功能化碳纳米管的开发,最大化利用CNT的自由基的清除潜力,以此维护人体健康。
总的来说,这种纳米技术可以彻底改变未来的医学治疗理念,为许多疑难杂症的治疗带来一线希望。但是,碳纳米管仍有许多重大的挑战和风险有待解决。
碳纳米管这一领域的研究仍处在起步阶段,但也取得了许多令人可喜的研究成果。科学家仍需要更多的想象力和创造力,来设计出不同的新型碳纳米管及其偶联物,使其具有更高效、安全的药用价值。
例如,未来制备的碳纳米管应附有新的敏感标记,以便它们可以直接到达靶细胞,这样科学家可以轻松地将它们从外部驱动到靶器官,以避免对其他健康组织产生副作用。
同时,这种纳米技术的许多缺陷机制必须有理论上的解释,特别是临床应用中需要关注的问题是CNT对人体健康产生的短期和长期影响。
一些有效的改进方法如下:通过细致谨慎地优化CNT物理和化学功能,减少CNT的毒性;同时对不同形式的碳纳米管进行更多的毒理学研究,包括从原始碳纳米管到功能化碳纳米管及其结合物;然后再对它们进行临床研究,从而对这种纳米技术的缺陷机制提供理论上的解释。
